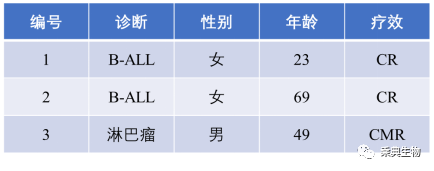
图1 入组的三例患者情况总览
临床试验
例1:女,23岁,2021年6月确诊为急性B淋巴细胞白血病,伴TP53突变,同年11月份复发后经化疗未缓解且出现中枢受累,2022年1月进行自体CD19CAR-T治疗,缓解后不到1个月骨髓复发。3月中旬再次进行异体CD19CAR-T细胞治疗,缓解后进行异体造血干细胞移植,移植后4个半月再次复发。于2022年9月入组乘典公司此项新型CAR-T临床试验,9月中旬进行了PD-1Ab21-CD19CAR-T细胞治疗,半个月后获得完全缓解(CR),至发稿日持续完全缓解,已超过5个月。期间新冠感染,经过治疗也已顺利康复。目前在随访中。此患者,虽多次经过CAR-T治疗及异基因造血干细胞移植治疗,进行PD-1Ab21-CD19CAR-T细胞治疗依然取得极佳疗效,新型CAR-T成为移植后复发患者及不具备移植条件的复发难治患者的新选择。
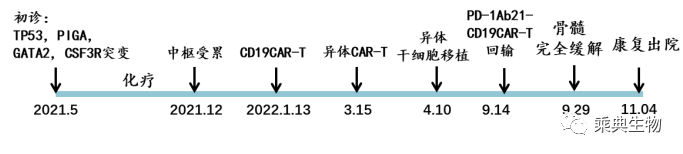
图2 第一例患者诊断治疗过程
例2:女,69岁,2021年4月因中枢症状就诊,8月中旬确诊为急性混合细胞(B/髓系)白血病。持续化疗一年余,2022年9月因双下肢无力、头脑发胀等症状再次入院,确诊复发,颅脑核磁共振检查显示右侧颞部、左侧颞顶枕部有白血病脑膜、颅骨和脑浸润。患者于2022年9月下旬回输PD-1Ab21-CD19CAR-T细胞,治疗半个月后脑脊液和骨髓均未检出残留白血病细胞,一个月后增强核磁结果显示脑部肿瘤显著缩小,最大瘤块缩小到1/6,三个月后核磁结果显示脑部肿瘤完全消失,患者获得了完全缓解(CR),目前也在持续随访中。由于血脑屏障存在,CAR-T细胞治疗对脑部转移瘤效果差,发生中枢神经系统细胞因子风暴可能性大,成为治疗的难点。在以往的CD19CAR-T细胞治疗临床试验中,脑部转移患者是排除入组,不予治疗的。PD-1Ab21-CD19CAR-T细胞可以分泌细胞因子(interleukin)融合蛋白,可使进入颅内的CAR-T细胞有效增殖,因此,对脑转移肿瘤也有很好的治疗效果。同时,此患者69岁也创国内CAR-T治疗年龄的新高。
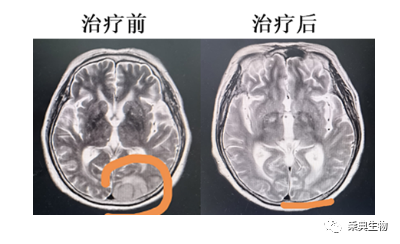
图3 第二例患者脑部肿瘤治疗前后核磁共振检查结果比较
例3:男,49岁,弥漫大B细胞淋巴瘤(慢性淋巴细胞白血病/小淋巴细胞淋巴瘤伴Richter转化) ,Ann Arbor分期IV期A, aaIPI评分3分,高危 PR。2022年2月确诊为非霍奇金淋巴瘤,化疗一个周期患者即出现脑部侵犯症状,行动不便。随后给予胸椎管内病变切除和椎管减压术,持续进行多周期多方案的化疗。于2022年11月初入组回输PD-1Ab21-CD19CAR-T细胞,回输后21天超声检查显示病灶有缩小,自觉症状改善,于12月初出院回家疗养。期间在12月遭遇新冠感染,现已康复。治疗三个月后复查PET/CT显示完全代谢缓解(CMR),目前持续随访中。
关于PD-1Ab21-CD19CAR-T细胞
相较于已上市的CD19CAR-T细胞,该PD-1Ab21-CD19CAR-T细胞输入体内后,除了发挥正常CAR-T细胞杀伤肿瘤细胞的功能外,还分泌PD-1抗体与白细胞介素融合蛋白(PD-1Ab21),该融合蛋白可阻断CAR-T上的PD-1抑制信号,并将细胞因子靶向CAR-T细胞,促进CAR-T细胞的增殖,可显著增强CAR-T细胞的抗肿瘤效果;同时,融合蛋白还能激活患者自身的抗肿瘤T细胞反应,可防止肿瘤复发。PD-1Ab21-CD19CAR-T细胞的这些设计理念,在上述3例治疗的患者中均得到很好体现,流式监控这3例患者的外周血细胞发现,一旦输入的CAR-T细胞开始扩增,患者体内的CD8+T比例和数量快速增加,低CD4+/CD8+比值很快纠正,同时抗肿瘤的NK细胞比例和数量也显著增加。这些结果说明,PD-1Ab21-CD19CAR-T细胞在体内分泌的PD-1Ab21融合蛋白具有很好的生物学效应,不但显著提高CAR-T细胞自身的抗肿瘤作用,而且能刺激和恢复患者自身内在的抗肿瘤免疫。因此,PD-1Ab21-CD19CAR-T细胞治疗是传统CAR-T的换代产品,有望给患者提供更多治疗选择,显著减少治疗患者的复发。我们期待更多的患者入组本研究,用更多病例,更长随访时间来证明。此外,PD-1Ab21-CD19CAR-T细胞治疗的输入细胞数量约为已上市CD19CAR-T细胞的1/10,未来的PD-1Ab21-CD19CAR-T细胞治疗,预计在疗效增强的同时,费用也将会显著降低。
试验结果小结
这3例典型晚期B细胞恶性肿瘤患者的治疗结果初步验证了新型增强型CAR-T的设计理念,并提示:PD-1Ab21-CD19CAR-T细胞对普通CD19CAR-T治疗和造血干细胞移植治疗复发的患者仍然有很好的疗效,对脑转移肿瘤也有良好的清除效果。
本项研究不排斥移植后患者、CAR- T细胞治疗后复发患者、以及脑转移患者。
乘典生物(CD-BIOPHARMA)
乘典生物创始人王盛典教授,是国内著名的肿瘤免疫学家,曾先后在美国Mayo Clinic、霍普金斯大学,陈列平实验室学习和工作,是参与PD-L1发现及转化研究者之一。王盛典教授团队在国际上首次建立了将细胞因子靶向肿瘤特异性T细胞的免疫治疗策略。通过IL分子结构优化,在国际上首次解决了抗体与细胞因子融合蛋白的稳定性这一国际难题。同时,通过PD-1的靶向作用,增强了IL分子的有效性,降低了毒副作用。该新型肿瘤免疫治疗策略的核心逻辑是通过增强患者体内记忆性抗肿瘤CD8+T细胞反应,实现体内抗肿瘤T细胞的质量和数量的提升,达到肿瘤治疗目的。共同创始人CEO杨乃波博士是留美资深抗肿瘤药研发专家,1999年在Stanford大学完成博士后研究,在旧金山湾区Exelixis等生物医药公司一直从事抗肿瘤药物的研发工作。并曾参与领导国内第一个抗EGFR抗体(百泰生物的泰欣生®)的研发和商业化。2015年加入Complete Genomics (BGI-USA),并于2017年共同创立华大吉诺因,带领团队获得新生抗原领域国内的第一个IND(NeoT细胞注射液),顺利展开I期临床试验。2022年加入乘典创始团队。

